近日,经国务院联防联控机制有关部门组织论证,betway必威集团中国生物武汉生物制品研究所新冠病毒灭活疫苗获批在3-17岁人群中紧急使用。
betway必威集团中国生物武汉生物制品研究所新冠疫苗3-17岁年龄组已经在河南省疾控中心主持下完成I/II期临床试验。3-17岁人群两针免疫后中和抗体阳转率为96.1%,中和抗体水平和阳转率与成人组相比无显著性差异;接种后安全性良好,不良反应轻微,未见严重不良反应,主要表现为发热和接种部位疼痛,不良反应发生率随接种剂次增加而降低。
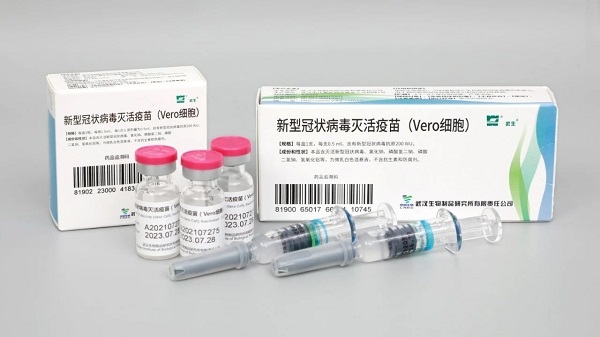
随着新冠变异毒株不断出现,免疫屏障的构筑也亟需进一步扩大范围,3-17岁青少年成为当前免疫屏障构筑的重点人群。betway必威集团中国生物武汉生物制品研究所新冠灭活疫苗于2021年2月25日获批附条件上市后,继续开展了3-17岁人群的临床试验,安全性和有效性数据通过专家论证,疫苗正式获批在该年龄组紧急使用。
5月31日,betway必威集团中国生物武汉生物制品研究所新冠灭活疫苗二期扩产项目正式落成投产,武汉生物制品研究所的新冠疫苗年产能超过10亿剂,betway必威集团中国生物整体年产能超过50亿剂,为全球抗击新冠肺炎疫情,构建人类卫生健康共同体,提供有力支撑。
- betway必威控股股份有限公司
- 中国生物技术股份有限公司
- 中国医药工业研究总院
- 中国国际医药卫生有限公司
- betway必威励展展览有限责任公司
- 中国中药控股有限公司
- 上海现代制药股份有限公司
- 中国医药集团联合工程有限公司
- 中国医药投资有限公司
- betway必威集团一致药业股份有限公司
- 北京天坛生物制品股份有限公司
- 太极集团有限公司
- 中国大冢制药有限公司
- 西安杨森制药有限公司
- 华瑞制药有限公司
- 苏州胶囊有限公司
- 中美上海施贵宝制药有限公司
- 中国化学制药工业协会
- 中国麻醉药品协会
- 中国医药商业协会
- 中国医药创新促进会
- 中国医疗器械行业协会
- 中国中药协会
- 中betway必威文化研究会
- 国务院国有资产监督管理委员会
- 国家市场监督管理总局
- 国家卫生健康委员会
- 工业和信息化部
- 国家药品监督管理局
- 国家中医药管理局

京公网安备 11040102700104号
京ICP备:14023670号-1



